セルファイン™ MAX Q-hv
セルファイン™ MAX ブチル HS
肺炎連鎖球菌は、世界中で特に子供や高齢者に高レベルの罹患率と死亡率を引き起こしている肺炎の主要な病原体の 1 つです。 最も重要な毒性因子の1つである細菌表面の莢膜多糖 (CPS) に基づく肺炎球菌ワクチンは、これらの感染症を予防するために使用されています。
莢膜多糖の精製に2段階のクロマトグラフィー精製を用いることで高純度にワクチンを精製することが可能です。このプロセスには、疎水性相互作用クロマトグラフィー (HIC) および陰イオン交換クロマトグラフィー (AEX) が用いられています。
このプロセスに最適化された 2つのクロマトグラフィー充填剤、セルファイン™ MAX ブチル HSとセルファイン™ MAX Q-hvを紹介します。
セルファイン™ MAX Q-hvの特徴Features
セルファイン™ MAX Q-hvは強陰イオン交換体です。セルファイン™の製品群には強陰イオン交換体がいくつかありますが、それらの比較を紹介します。 セルファイン™ MAX Q-hvは莢膜多糖の精製に最適化するためリガンド濃度を最適化しています。
| セルファイン™ MAX Qシリーズの比較 | |||
|---|---|---|---|
| グレード | セルファイン™ MAX Q-r | セルファイン™ MAX Q-h | セルファイン™ MAX Q-hv |
| ベース担体 | デキストラン修飾された高度架橋セルロース粒子 | ||
| 粒径 | ca. 40~130 μm | ||
| 官能基 (リガンド) | 強陰イオン / -N+(CH3)3 | ||
| イオン交換容量 (meq/ml) | 0.10~0.20 | 0.13~0.22 | 0.04~0.07 |
| 動的吸着量 BSA (mg/ml) | 110 | 180 | 120 |
| 操作流速 | 600 cm/h(0.3 MPa) I.D.30 cm-L20 cm、移動相:純水 24 ºC | ||
| pH 安定性 | pH 2 - 12 | ||
| 化学安定性 | 一般的に使用されるバッファーで安定 | ||
| 定置洗浄 | 1 M NaOH | 0.5 M NaOH | |
| 包装形態 | 20% エタノールに懸濁 | ||
セルファイン™ MAX ブチル HSの特徴Features
セルファイン™ MAX ブチル HSはブチル基を有する疎水性担体です。セルファイン™の製品群には疎水性担体がいくつかありますが、それらの比較を紹介します。 セルファイン™ MAX ブチル HSは莢膜多糖の精製に最適化するためリガンド濃度を最適化しています。
| セルファイン™ MAX ブチルシリーズの比較 | ||
|---|---|---|
| グレード | セルファイン™ MAX ブチル | セルファイン™ MAX ブチル HS |
| ベース担体 | 高度架橋セルロース | |
| 粒径 | ca. 40~130 μm | |
| 官能基 (リガンド) | 低濃度ブチル基 | 高濃度ブチル基 |
| BSA吸着量 (mg/ml) | 9 | 13 |
| BSA溶出効率 (%) | 70 | 36 |
| 操作圧力 | <0.3 MPa | |
| pH 安定性 | pH 2 - 13 | |
| 化学安定性 | 一般的に使用されるバッファーで安定 | |
| 定置洗浄 | 1 M NaOH | |
| 包装形態 | 20% エタノールに懸濁 | |
セルファイン™ MAX ブチル HSの分離特性Model Protein Separation
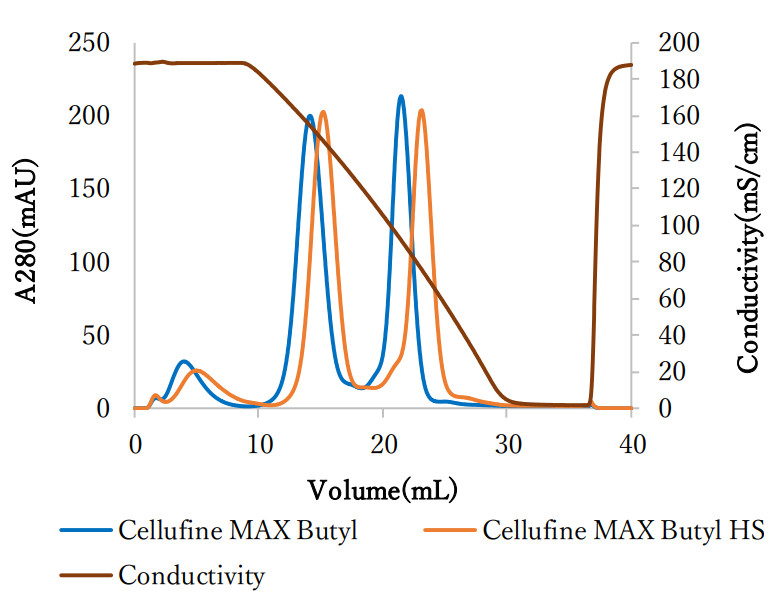
- カラム
- 6.6 mm ID x 30 mmL (1.0 ml)
- バッファー A
- 10 mMリン酸Na, 1.5 M硫酸アンモニウム, pH 7.0
- バッファー B
- 10 mMリン酸Na, pH 7.0
- タンパク質
- リボヌクレアーゼA, シトクロムC, リゾチーム
セルファイン™ MAX ブチル HSの流速特性Pressure vs. Flow Properties
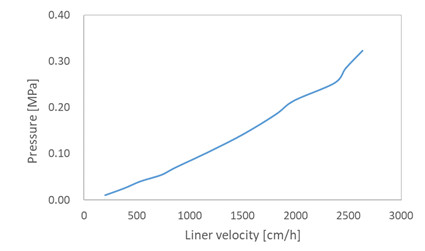
- カラム
- 2.2cm I.D. x 20 cm L
- 温度
- 24 ± 1 ℃
- 移動相
- 純水
Streptococcus pneumoniae血清型19Fの莢膜多糖類の精製
肺炎連鎖球菌は、世界中で特に子供や高齢者に高レベルの罹患率と死亡率を引き起こしている肺炎の主要な病原体の 1 つです。 最も重要な毒性因子の1つである細菌表面の莢膜多糖 (CPS) に基づく肺炎球菌ワクチンは、これらの感染症を予防するために使用されています。 従来のエタノール沈殿は、ほとんどの血清型に適したCPSを精製するための一般的なプロセスです。 ただし、それらは複雑で時間がかかります。その結果、肺炎球菌ワクチンは非常に高価となります。 これらの欠点を克服するために、多くの改善されたプロセスが提案されています。これらのプロセスのいくつかには、クロマトグラフィープロセスが含まれます。 ここでは、エタノール沈殿のないCPSの単純化された2段階クロマトグラフィー精製プロセスを提案します。 このプロセスには、疎水性相互作用クロマトグラフィー (HIC) および陰イオン交換クロマトグラフィー (AEX) が用いられています。 このプロセスに最適化された 2つのクロマトグラフィー担体セルファイン™ MAX ブチル HSとセルファイン™ MAX Q-hvを紹介します。

| 多糖類 回収率% | 多糖類 純度% | タンパク質μg/mL | 核酸μg/mL | タンパク質/多糖類% | 核酸/多糖類% | |
|---|---|---|---|---|---|---|
| ロードサンプル | - | 46 | 73 | 772 | 10 | 106 |
| MAXブチル HS精製後 | 89 | 54 | M.D. | 436 | 0 | 84 |
| MAX Q-hv精製後 | 98 | 99 | N.D. | 4 | 0 | 1 |
化学的安定性Chemical and Caustic Stability
以下の溶媒、オートクレーブに対して安定です。
- エタノール (70%)
- 水酸化ナトリウム (0.5M)
- イソプロパノール (30%)
- 界面活性剤
- グアニジン塩酸塩 (6M)
- オートクレーブ (121 ºC, 20 min)
- 尿素 (6M)
- セルファイン™ MAX ブチル HS
- セルファイン™ MAX Q-hv
